2021年7月29日,药物研究所邹敏等在Web of Science数据库Q1区Bioorganic Chemistry(影响因子:IF 5.275)杂志发表题为“Design, synthesis and anticancer evaluation of new 4-anilinoquinoline-3-carbonitrile derivatives as dual EGFR/HER2 inhibitors and apoptosis inducers”的研究性文章。邹敏副研究员为第一作者,郑立运研究员为通讯作者。郑州大学/河南省医药科学研究院为第一通讯单位。
针对EGFR/HER2双靶点抑制剂可能在非小细胞肺癌、胃癌、结肠癌、食管癌等恶性肿瘤治疗中,发挥协同作用及低毒副作用的优点。为了探寻新型HER2/EGFR双靶点抑制剂,郑立运团队基于erlotinib 和EGFR蛋白酶的共晶结构(PDB ID:1M17),建立衍生物和HER2的同源模型,将4-氨基喹啉-3-甲腈衍生物置于靶酶键合位置,4位的芳氨基位于蛋白酶残基组成的疏水性口袋可进一步加强衍生物与EGFR/HER2 靶酶的键合作用,C-7 和 C-6的侧链朝向键合位置的开口处,由此推断,对6,7位侧链的修饰可以改变衍生物的物理化学性质,进而影响其生物活性。团队在6位引入各种极性或非极性基团设计合成了12种化合物,进行EGFR/HER2抑制性评价和体外对EGFR/HER2过表达细胞株抗增殖活性评价,分析了各种取代基团对活性的影响。进一步探讨活性优异的衍生物6d对细胞凋亡和周期的影响,并通过分子模型对接探讨衍生物和靶酶的相互作用(见图),衍生物6d可以作为的EGFR /HER2抑制剂先导化合物进一步深入研究。本研究发现了新型的EGFR/HER2双靶点肿瘤抑制剂,也为开发新型抗肿瘤药物奠定坚实基础。
这项研究工作得到了河南省科技攻关项目及院基本科研业务费资助。
文章(Bioorganic Chemistry,114 (2021) 105200)链接:https://doi.org/10.1016/j.bioorg.2021.105200

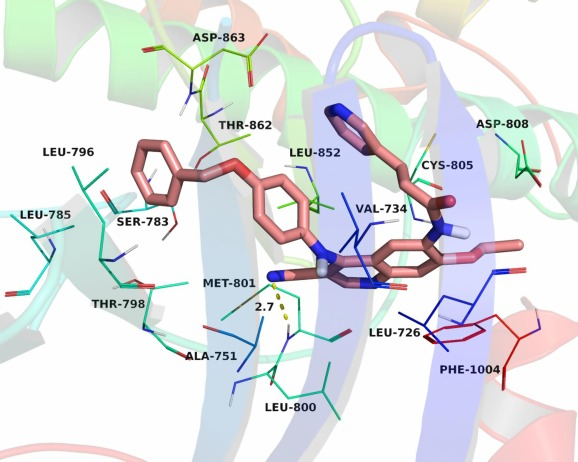
图 衍生物6d和EGFR及HER2的作用模式
(邹敏供稿)

